La fenilalanina, la tirosina y el triptófano, corresponden a los aminoácidos aromáticos. En este grupo, sólo la tirosina es un aminoácido no esencial (que los mamíferos pueden sintetizar a partir del consumo de la fenilalanina), mientras que la fenilalanina y el triptófano son aminoácidos esenciales, esto quiere decir que los mamíferos no pueden sintetizarlos y deben obtenerlos de los alimentos. Para la formación del anillo bencénico de estos aminoácidos, se lleva a cabo la ruta del shikimato para la formación del corismato, esta ruta la llevan a cabo tanto plantas como microorganismos. (Rodríguez Salinas, 2019).
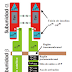
La ruta del shikimato comienza con la condensación de la eritrosa-4-fosfato (deriva de la ruta de las pentosas fosfato) y el fosfoenolpiruvato (derivado de la ruta glucolítica), para formar el 2-ceto-3-desoxiarabino-heptulosonato-7-fosfato (DAHP) por medio de la DAHP sintasa. Después, por medio de la 3-DHG sintasa se forma el 3-dehidroquinato el cual se deshidrata para formar el 3-deshidroshikimato por medio de la DHQ deshidratasa. Luego, por medio de la shikimato deshidrogenasa, se forma el ácido shikímico y una vez formado, reacciona con la shikimato quinasa para producir el shikimato-3-fosfato, que después se convierte en 5-enolpiruvilshikimato-3-fosfato (EPSP) por la EPSP sintasa. Finalmente, el EPSP se convierte en corismato por la corismato sintasa. (Rodríguez Salinas, 2019).
 |
| Figura 1. Ruta del shikimato y obtención del corismato. Recuperado de: https://es.wikipedia.org/wiki/Ruta_del_%C3%A1cido_shik%C3%ADmico |
El corismato se convierte en prefenato, que es el precursor de la fenilalanina y de la tirosina; y en antranilato, que es el precursor del triptófano. El corismato, por medio de la corismato mutasa, se convierte en prefenato y este luego en arogenato por la prefenato aminotransferasa. El arogenato pasa por una descarboxilación oxidativa por medio de la arogenato deshidrogenasa para formar la tirosina; o se deshidrata por medio de la arogenato deshidratasa para formar fenilialanina. Existen dos rutas alternas para la producción de estos aminoácidos, en una de ellas, ocurre una descarboxilación oxidativa del prefenato por medio de la prefenato deshidrogenasa para producir 4-hidroxifenilpiruvato; o también el prefenato por medio de la prefenato deshidratasa, se deshidrata para formar el fenilpiruvato. Después ocurre una transaminación de estos productos para formar tirosina a partir del 4-hidroxifenilpiruvato y fenilalanina del fenilpiruvato. Para el triptófano, el antranilato se convierte en indolglicerol fosfato que después por medio de la triptófano sintasa genera el triptófano. (Rodríguez Salinas, 2019).
 |
| Figura 2. Obtención de fenilalanina y tirosina a partir del corismato. Recuperado de:http://eprints.uanl.mx/18341/1/1080289155.pdf |
 |
| Figura 3. Obtención de triptófano a partir del corismato. Recuperado de: https://www.pngwing.com/es/free-png-kaqzz |
La histidina es un aminoácido esencial, puede ser sintetizada por la mayoría de los microorganismos, en una ruta compleja que parte de ribosa 5-fosfato y tiene 11 pasos metabólicos. La vía comienza con la formación de 5-fosforribosil-1-pirofosfato (PRPP) a partir de ribosa 5-fosfato y ATP, catalizada por la PRPP sintetasa. El siguiente paso está catabolizado por la fosforribosil transferasa, con incorporación de ATP, para formar N1-(5'-fosforribosil)-ATP; compuesto que experimenta la pérdida del pirofosfato, una deshidratación y una isomerización para formar N1-(5'-fosforribosilformimino)-5-aminoimidazol-4-carboxamida-1-ribonucleótido que, por eliminación de 5-aminoimidazol-4-carboxamida-1-ribonucleótido y entrada de nitrógeno procedente de la glutamina, da lugar a imidazol glicerol fosfato que, tras diversos pasos metabólicos, que incluyen transaminación y oxidación, origina histidina. La histidina es un retroinhibidor alostérico de la fosforribosil transferasa, que cataliza la primera etapa específica de su biosíntesis (Teijón et al., 2006).
 |
| Figura 4. Síntesis de la histidina. Recuperado de: Teijón et al., 2006. |
Funciones de los aminoácidos aromáticos e histidina:
- Es precursora de aminoácidos metilados como la lisina, alanina, metionina, asparagina, ácido aspártico y arginina.
- Debido a su capacidad catalítica se encuentra presente en el sitio activo de varias enzimas asociadas a la transferencia de electrones. (Cervantes y colaboradores, 2017)
- Mejora la respuesta inmunitaria.
- Ayuda en la disminución de los efectos negativos de la artritis reumatoide (falta de movilidad, inflamación).
- Mantenimiento de las vainas de mielina.
- Importante en la producción de eritrocitos y leucocitos.
- Reduce presión arterial.
- Utilizada como neuromodulador. (Honores, 2013)
- La tirosina está muy relacionada con la fenilalanina, y es usada en una manera muy similar a la producción de las catecolaminas.
- Es considerado un nutriente anabólico (favorecen acumulación de proteína y disminuyen deposición de grasa).
- Colabora en la síntesis de neurotransmisores como la epinefrina y la dopamina.
- Importante en la producción de células rojas y blancas.
- Importante colaborador de la actividad de las glándulas pituitarias, tiroidea y adrenal.
- Neutraliza radicales libres.
- Junto con el yodo participa en la síntesis de la tiroxina.
- Importante colaborador en la producción de melanina y adrenalina. (Colastra, 2013)
- El triptófano es un aminoácido esencial precursor de la serotonina y la melatonina. La serotonina es un neurotransmisor implicado en la regulación del humor y el estado de ánimo, y la melatonina es una hormona reguladora de los ciclos de vigilia y sueño (Belaustegui, 2019).
- El hígado también puede utilizar el triptófano para producir niacina (vitamina B3), la cual es necesaria para el metabolismo energético y la producción de ADN (Bridges, 2020).
- Ayuda a aliviar el dolor.
- Ayuda en la prevención y tratamiento de la depresión, elevando el estado de ánimo.
- Puede estar relacionada con el sentimiento de estar enamorado.
- Actúa como un estimulante cerebral.
- Ayuda a incrementar los niveles de endorfinas.
- Nos ayuda a regular el ritmo cardiaco.
- Ayuda en resolver problemas de pigmentación de la piel ya que interviene en la producción del colágeno, fundamentalmente en la estructura de la piel y el tejido conectivo.
- Ayuda a reducir la sensación de apetito.
- Ayuda a disminuir los síntomas de algunas enfermedades neurológicas ya que participa en la formación de diversas neurohormonas.
- Promueve el estado de alerta y la vitalidad.
- Ayuda a la memoria y el aprendizaje (EcuRed colaboradores, 2019).
Referencias bibliográficas
Belaustegui,
I. (2019). Triptófano: ¿Qué es y por qué funciona?. Recuperado el 22 de junio
de 2021, de: https://www.vidapotencial.com/triptofano/#Que_funciones_tiene_el_triptofano
Bridges, M. (2020). Triptófano. Recuperado
el 22 de junio de 2021, de: https://medlineplus.gov/spanish/ency/article/002332.htm
Cervantes,
K., Mejía, I., Villanueva, P., Donovan, O., Colín, M., y Heredia, A. (2017). La
histidina como un posible precursor en el origen de la vida. Revista
de Ciencias de la Vida, 26(2). Recuperado el 21 de junio de 2021, de: https://www.redalyc.org/jatsRepo/4760/476052525001/476052525001.pdf
Colestra, J. (2013). La Tirosina.
Lamberts Española S.L. Recuperado el 22 de junio de 2021, de: https://lambertsusa.com/art-dsp/la-tirosina/
EcuRed colaboradores. (2019). Fenilalanina. Recuperado el 22 de junio de 2021, de: https://www.ecured.cu/Fenilalanina#Funciones_en_el_organismo
Honores, J. (2013). Aminoácidos y
proteínas. Universidad Técnica de Machala. Recuperado el 21 de junio de
2021, de: https://es.slideshare.net/jessymontalvan/la-histidina
Rodríguez Salinas, P. A. (2019). Caracterización
del contenido nutricional, compuestos polifenólicos y capacidad antioxidante de
maíces pigmentados (Zea mays L.) nativos del sur de Nuevo León. [Tesis
de doctorado]. Universidad Autónoma de Nuevo León.
Teijón, J., Garrido, A., Blanco, D.,
Villaverde, C., Mendoza, C. & Ramírez, J. (2006). Fundamentos de
bioquímica metabólica (3ra ed.). Madrid: Editorial Tébar, pp.
208-215.